Glaskörperinjektionen Intravitreale Injektionen (IVOM)
Auch intravitreale operative Medikamentengabe (IVOM) genannt ist eine Behandlungsmethode bei der verschiedene Medikamente meist ambulant unter operativen Bedingungen ins Augeninnere (Glaskörper) eingespritzt werden. Sie zählt zu den modernsten Therapiemethoden bei Netzhaut-, Makula- und Glaskörpererkrankungen. Die Ärzte der DOmed-Augenzentren empfehlen eine IVOM-Behandlung bei akuten therapiebedürftigen Zuständen der folgenden Erkrankungen:
Behandlungsablauf einer IVOM
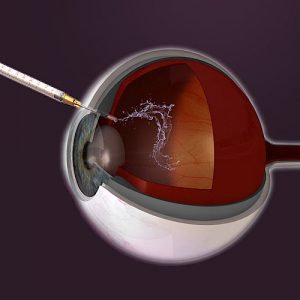
Nach einer lokalen Betäubung wird das Medikament mittels einer hauchdünnen Kanüle ca. 6mm tief in den Glaskörper eingespritzt. Neben der einfachen Medikamentenverabreichung kann auch ein Implantat in das Auge eigesetzt werden, welches den Wirkstoff über einen längeren Zeitraum gleichmäßig abgibt. Dies reduziert besonders bei chronisch kranken Patienten die Anzahl der benötigten Eingriffe. Besonderer Vorteil einer IVOM ist eine drastische Reduzierung möglicher Nebenwirkungen, da es sich hierbei um eine lokale Anwendung handelt, die nur eine möglichst geringe Dosierung der Wirkstoffe benötigt.
VEGF-Blocker gegen AMD und diabetische Retinopathie
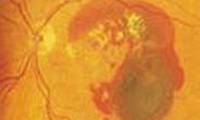
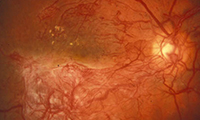
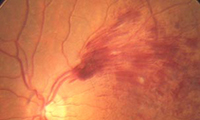
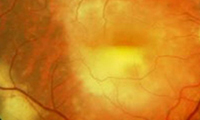
Die feuchte altersbedingte Makuladegeneration war lang Zeit für die Hälfte aller Erblindungen verantwortlich. Die Einführung der Therapie mit Medikamenteninjektionen in den Glaskörper haben die Aussichten der Betroffenen erheblich verbessert: Sogenannte VEGF-Hemmer stoppen durch die Blockade des Vascular Endothelial Growth Factor (VEGF) das Gefäßwachstum (Angiogenese).
Sie ermöglichte es, dass bei einem Großteil der Patienten mit später altersbedingter Makuladegeneration die fortschreitende Sehverschlechterung aufgehalten werden und sich bei ca. 50 Prozent der Betroffenen die Sehqualität verbessern kann. Zerstörte Areale der Netzhaut sind allerdings auch mit dieser Methode nicht wieder herzustellen.
Für die Behandlung kommen verschiedene Medikamente in Frage:
Vabysmo® ist seit September 2022 für Erwachsene zur Behandlung der neovaskulären (feuchten) altersabhängigen Makuladegeneration (nAMD) und diabetischem Makulaödem (DMÖ) zugelassen. Es handelt sich um den ersten bispezifischen Antikörper, der für die intraokulare Anwendung entwickelt wurde.
Brolucizumab ist in Europa seit 2020 zur Behandlung der neovaskulären (feuchten) altersbedingten Makuladegeneration (AMD) und zur Behandlung einer Visusbeeinträchtigung infolge eines diabetischen Makulaödems (DMÖ) bei Erwachsenen zugelassen.
Seit November 2012 ist das Medikament in Deutschland für die Anwendung im Auge bei Erwachsenen zugelassen. Dieses Medikament ist, genau wie Lucentis®, speziell für die Therapie im Auge entwickelt worden und trägt den Handelsnamen Eylea®. Der Wirkmechanismus von Aflibercept ist der Gleiche wie bei dem 2007 zugelassen Ranibizumab (Lucentis®). Eylea® ist für die Behandlung der feuchten AMD, diabetische Makulaödem, chorioidale Neovaskularisation bei hoher Myopie und Makulaödem bei VAV/ZVV bei Erwachsenen zugelassen.
Seit Februar 2007 ist in Deutschland ein vom Bevacizumab (Avastin®) (s. unten) abgeleitetes Medikament, Ranibizumab speziell für die Anwendung im Auge zugelassen. Dieses Medikament wird unter dem Handelsnamen Lucentis® vertrieben und wurde speziell für die Therapie im Auge entwickelt. Lucentis® ist für die Behandlung der feuchten AMD, diabetische Makulaödem, Makulaödem bei VAV/ZVV, chorioidale Neovaskularisation bei hoher Myopie und bei chorioidale Neovaskularisation in Verbindung mit seltenen Erkrankungen zuglassen.
Dieses dem Lucentis® (Ranibizumab) verwandte Medikament wird seit 2005 in Deutschland und weltweit bei der feuchten AMD häufig und mit positiven Behandlungsergebnissen eingesetzt. Bevacizumab wurde ursprünglich zur Tumorbehandlung entwickelt (auch hier wachsen neue Blutgefäße) und ist unter dem Namen Avastin® für die Behandlung verschiedener Tumorerkrankungen zugelassen. Bei der Verwendung von Avastin® handelt es sich um einen sog. „off-label use“, d.h. eine Verwendung des Medikaments in einem arzneimittelrechtlich nicht zugelassenen Anwendungsgebiet. Dies bedeutet allerdings nicht, dass Ärzte das Medikament am Auge nicht verwenden dürfen.
Ozurdex® ist ein Medikamententräger, der nach Einbringung in das Augeninnere über einen längeren Zeitraum (4-6 Monate) den Wirkstoff Dexamethason, ein Corticoid, abgibt. Seit 2010 ist in Deutschland das Medikament Ozurdex® (Dexamethason-lmplantat) speziell für die Anwendung im Auge für die Behandlung des Makulaödems bei retinalen Venenverschlüssen, diabetischem Makulaödem, und seit 2011 für die Behandlung des Makulaödems bei Uveitis intermedia/posterior zugelassen.
Iluvien® ist für eine „second line“-Therapie zur Behandlung von Sehstörungen in Verbindung mit chronischem diabetischem Makulaödem indiziert, welche auf andere verfügbare Therapien nur unzureichend ansprechen.